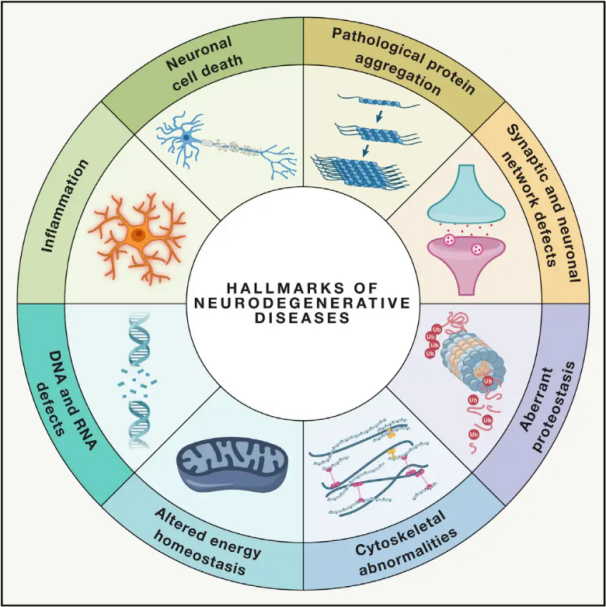
נעוראָדעגענעראַטיווע קראַנקייטן(NDDs) ווערן כאראקטעריזירט דורך דעם פראגרעסיוון אדער אנהאלטנדיקן פארלוסט פון ספעציפישע שוואכע נעוראנאלע פאפולאציעס אין מוח אדער רוקן-מארך. די קלאסיפיקאציע פון NDDs קען זיין באזירט אויף פארשידענע קריטעריעס, אריינגערעכנט די אנטאמאטישע פארשפרייטונג פון נעוראדעגענעראציע (אזוי ווי עקסטראפיראמידאלע דיסאָרדערס, פראנטאטעמפאראלע דעגענעראציע, אדער ספּינאסערעבעלארע אטאקסיעס), ערשטיקע מאלעקולארע אומנארמאלקייטן (ווי אמילאיד-β, פריאנען, טאו, אדער α-סינוקלעין), אדער הויפט קלינישע שטריכן (אזוי ווי פארקינסאן'ס קרענק, אמיאטראפישע לאַטעראלע סקלעראזיס, און דעמענץ). טראץ די אונטערשיידן אין קלאסיפיקאציע און סימפטאם פרעזענטאציע, טיילן דיסאָרדערס ווי פארקינסאן'ס קרענק (PD), אמיאטראפישע לאַטעראלע סקלעראזיס (ALS), און אַלזשיימערס קרענק (AD) געמיינזאמע אונטערלייגנדיקע פראצעסן וואס פירן צו נעוראנאלע דיספונקציע און עווענטועל צעל טויט.
מיט מיליאָנען וועלט-ברייט באַטראָפן דורך NDDs, שאַצט די וועלט געזונטהייט אָרגאַניזאַציע אַז ביז 2040 וועלן די קראַנקייטן ווערן די צווייטע גרעסטע סיבה פון טויט אין אַנטוויקלטע לענדער. כאָטש עס זענען פאַרשידענע באַהאַנדלונגען בנימצא צו פֿאַרלייכטערן און פאַרוואַלטן די סימפּטאָמס פֿאַרבונדן מיט ספּעציפֿישע קראַנקייטן, בלייבן עפעקטיווע מעטאָדן צו פאַרלאַנגזאַמען אָדער היילן די פּראָגרעס פון די צושטאנדן שווער צו דערגרייכן. לעצטע שטודיעס ווייַזן אויף אַ ענדערונג אין באַהאַנדלונג פּאַראַדיגמען פון בלויז סימפּטאָמאַטיש פאַרוואַלטונג צו נוצן צעל פּראַטעקטיוו מעקאַניזאַמז צו פאַרמייַדן ווייטערדיקע דיטיריעריישאַן. ברייטע באַווייַזן סאַגדזשעסט אַז אָקסידאַטיוו דרוק און אָנצינדונג שפּילן וויכטיקע ראָלעס אין נעוראָדעגענעריישאַן, פּאַזישאַנינג די מעקאַניזאַמז ווי קריטישע צילן פֿאַר צעלולאַר פּראַטעקשאַן. אין די לעצטע יאָרן, יסודותדיקע און קלינישע פאָרשונג האט אַנטפּלעקט דעם פּאָטענציעל פון היפּערבאַריק זויערשטאָף טעראַפּיע (HBOT) אין באַהאַנדלונג פון נעוראָדעגענעראַטיווע קראַנקייטן.
פֿאַרשטיין היפּערבאַרישע זויערשטאָף טעראַפּיע (HBOT)
HBOT טיפּיש באַשטייט פון העכער 1 אַבסאָלוטע אַטמאָספֿערע (ATA) — דער דרוק אויף ים־שפּיגל — פֿאַר אַ געדויער פֿון 90-120 מינוט, אָפֿט פֿאָדערנדיק קייפל סעסיעס לויטן ספּעציפֿישן צושטאַנד וואָס ווערט באַהאַנדלט. דער פֿאַרשטאַרקטער לופֿט־דרוק פֿאַרבעסערט די צושטעל פֿון זויערשטאָף צו צעלן, וואָס אין דער ריי סטימולירט שטאַם־צעל פּראָליפֿעראַציע און פֿאַרשטאַרקט די היילונג־פּראָצעסן וואָס ווערן געפֿירט דורך געוויסע וואוקס־פֿאַקטאָרן.
אריגינעל, איז די אנווענדונג פון HBOT געווען באזירט אויף דעם בויל-מעריאט געזעץ, וואס שטעלט פאר די דרוק-אפהענגיקע רעדוקציע פון גאז באבלס, צוזאמען מיט די בענעפיטן פון הויכע זויערשטאף לעוועלס אין געוועבן. עס איז דא א רייע פון פאטאלאגיעס באקאנט צו נוץ האבן פון דעם היפעראקסישן צושטאנד פראדוצירט דורך HBOT, אריינגערעכנט נעקראטישע געוועבן, ראדיאציע שאדנס, טראומא, פארברענטע געוועבן, קאמפארטמענט סינדראם, און גאז גאַנגרענע, צווישן אנדערע ליסטעד דורך די אונטערסי און היפערבאַריק מעדיקאַל געזעלשאפט. באמערקענסווערט, האט HBOT אויך געוויזן עפעקטיווקייט אלס א צוגאב באהאנדלונג אין פארשידענע אנטצינדליכע אדער אינפעקציעזע קראנקהייט מאדעלן, ווי קאליטיס און סעפּסיס. געגעבן זיינע אנטי-אנטצינדליכע און אקסידאטיוו מעכאניזמען, אָפערט HBOT א באדייטנדיקן פאטענציאל אלס א טעראפויטישע וועג פאר נעוראדעגענעראטיווע קראנקהייטן.
פּרעקלינישע שטודיעס פון היפּערבאַריש זויערשטאָף טעראַפּיע אין נעוראָדעגענעראַטיווע קראַנקייטן: ינסייץ פון די 3×Tg מויז מאָדעל
איינע פון די באַמערקנסווערטע שטודיעספאָקוסירט אויף דעם 3×Tg מויז מאָדעל פון אַלצהיימערס קרענק (AD), וואָס האָט געוויזן דעם טעראַפּעווטישן פּאָטענציאַל פון HBOT אין פֿאַרבעסערן קאַגניטיווע דעפיציטן. די פאָרשונג האָט אַרייַנגענומען 17-חודש-אַלטע זכר 3×Tg מײַז קאַמפּערד צו 14-חודש-אַלטע זכר C57BL/6 מײַז וואָס האָבן געדינט ווי קאָנטראָלן. די שטודיע האָט דעמאָנסטרירט אַז HBOT ניט בלויז פֿאַרבעסערט קאַגניטיווע פֿונקציע, נאָר אויך באַדײַטנד רידוסט אָנצינדונג, פּלאַק לאָוד, און טאַו פאָספאָרילאַציע - אַ קריטישער פּראָצעס פֿאַרבונדן מיט AD פּאַטאַלאַדזשי.
די פּראַטעקטיוו ווירקונגען פון HBOT זענען צוגעשריבן געוואָרן צו אַ פאַרקלענערונג אין נעוראָ-אָנצינדונג. דאָס איז באַוויזן געוואָרן דורך דער רעדוקציע פון מיקראָגליאַל פּראָליפעראַציע, אַסטראָגליאָסיס, און די סעקרעציע פון פּראָ-ינפלאַמאַטאָרישע ציטאָקינען. די רעזולטאַטן אונטערשטרייַכן די צווייפאַכיקע ראָלע פון HBOT אין פֿאַרבעסערן קאַגניטיוו פאָרשטעלונג בשעת גלייכצייטיג פֿאַרמינדערן נעוראָ-ינפלאַמאַטאָרישע פּראָצעסן פֿאַרבונדן מיט אַלצהיימערס קרענק.
נאך א פּרעקליניש מאָדעל האט גענוצט 1-מעטהיל-4-פעניל-1,2,3,6-טעטראַהידראָפּירידין (MPTP) מײַז צו עוואַלויִרן די פּראַטעקטיוו מעקאַניזמען פון HBOT אויף נעוראָנאַל פונקציע און מאָטאָרישע מעגלעכקייטן. די רעזולטאַטן האָבן געוויזן אַז HBOT האָט בייגעטראָגן צו פֿאַרבעסערטע מאָטאָרישע אַקטיוויטעט און גריפּ שטאַרקייט אין די מײַז, וואָס קאָרעלירט מיט אַ פאַרגרעסערונג אין מיטאָטשאָנדריאַל ביאָגענעסיס סיגנאַלינג, ספּעציפֿיש דורך די אַקטיוואַציע פון SIRT-1, PGC-1α, און TFAM. דאָס אונטערשטרייכט די באַדײַטנדיקע ראָלע פון מיטאָטשאָנדריאַל פונקציע אין די נעוראָפּראָטעקטיוו יפעקס פון HBOT.
די מעכאניזמען פון HBOT אין נעוראָדעגענעראַטיווע קראַנקייטן
דער אונטערליגנדיקער פּרינציפּ פון נוצן HBOT פֿאַר NDDs ליגט אין דער באַציִונג צווישן פאַרקלענערטער זויערשטאָף צושטעל און די סאַסעפּטאַבילאַטי צו נעוראָדעגענעראַטיווע ענדערונגען. היפּאָקסיאַ-ינדוסאַבאַל פאַקטאָר-1 (HIF-1) שפּילט אַ צענטראַלע ראָלע ווי אַ טראַנסקריפּציע פאַקטאָר וואָס ענייבאַלז צעלולאַרע אַדאַפּטאַציע צו נידעריק זויערשטאָף דרוק און איז געווען ימפּליקייטיד אין פאַרשידענע NDDs אַרייַנגערעכנט AD, PD, האַנטינגטאָן ס קרענק, און ALS, מאַרקינג עס ווי אַ קריטיש מעדיצין ציל.
צוליב דעם וואָס עלטער איז אַ באַדייטנדיקער ריזיקאָ־פאַקטאָר פֿאַר פֿאַרשידענע נעוראָדעגענעראַטיווע קרענק, איז עס וויכטיק צו אויספֿאָרשן דעם איינפֿלוס פֿון HBOT אויף אַלטערנדיקער נעוראָביאָלאָגיע. שטודיעס האבן געוויזן אז HBOT קען פארבעסערן עלטער-פארבונדענע קאגניטיוון דעפיציטן אין געזונטע עלטערע סוביעקטן.דערצו, עלטערע פּאַציענטן מיט באַדייטנדיקע זכּרון פּראָבלעמען האָבן אויסגעוויזן קאַגניטיווע פֿאַרבעסערונגען און געוואקסענעם סערעבראַלן בלוט שטראָם נאָך ויסשטעלן צו HBOT.
1. השפּעה פון HBOT אויף אָנצינדונג און אָקסידאַטיוו סטרעס
HBOT האט דעמאנסטרירט די מעגלעכקייט צו פארלייכטערן נעוראָאינפֿלאַמאַציע אין פּאַציענטן מיט שווערע מוח דיספֿונקציע. עס פארמאגט די קאַפּאַציטעט צו אַראָפּרעגולירן פּראָ-ינפֿלאַמאַטאָרישע ציטאָקינען (אַזאַ ווי IL-1β, IL-12, TNFα, און IFNγ) בשעת עס ארויפרעגולירט אַנטי-ינפֿלאַמאַטאָרישע ציטאָקינען (ווי IL-10). עטלעכע פֿאָרשער פֿאָרשלאָגן אַז רעאַקטיווע זויערשטאָף מינים (ROS) דזשענערייטאַד דורך HBOT מעדיאַטירן עטלעכע נוציקע יפעקס פון דער טעראַפּיע. דעריבער, חוץ זיין דרוק-אָפּהענגיק בלאָז-רעדוצירנדיק קאַמף און די דערגרייכן פון הויך געוועב זויערשטאָף זעטיקונג, די positive רעזולטאַטן לינגקט צו HBOT זענען טיילווייז אָפענגיק אויף די פיזיאַלאַדזשיקאַל ראָלעס פון די פּראָדוצירט ROS.
2. ווירקונגען פון HBOT אויף אַפּאָפּטאָסיס און נעוראָפּראָטעקשאַן
פאָרשונג האט געוויזן אַז HBOT קען רעדוצירן היפּאָקאַמפּאַל פאָספאָרילאַציע פון p38 מיטאָגען-אַקטיווייטיד פּראָטעין קינאַזע (MAPK), דערנאך פֿאַרבעסערן קאַגנישאַן און פאַרקלענערן היפּאָקאַמפּאַל שאָדן. ביידע אַליין HBOT און אין קאָמבינאַציע מיט גינקאָ בילאָבאַ עקסטראַקט זענען געפֿונען צו נידעריקער די אויסדרוק פון Bax און די טעטיקייט פון קאַספּאַסע-9/3, ריזאַלטינג אין פאַרקלענערט אַפּאָפּטאָסיס ראַטעס אין ראָודאַנט מאָדעלס ינדוסט דורך aβ25-35. דערצו, אן אנדער לערנען האט דעמאַנסטרירט אַז HBOT פּריקאַנדישאַנינג ינדוסט טאָלעראַנץ קעגן סערעבראַל ישעמיאַ, מיט מעקאַניזאַמז ינוואַלווינג געוואקסן SIRT1 אויסדרוק, צוזאַמען מיט פאַרגרעסערטע B-צעל לימפאָמאַ 2 (Bcl-2) לעוועלס און רידוסט אַקטיוו קאַספּאַסע-3, אונטערשטרייכן HBOT ס נעוראָפּראָטעקטיוו און אַנטי-אַפּאָפּטאָטיק פּראָפּערטיעס.
3. איינפלוס פון HBOT אויף צירקולאציע אוןנעוראָגענעסיס
אויסשטעלן סוביעקטן צו HBOT איז פארבונדן מיט פארשידענע עפעקטן אויף די קראַניאַלע וואַסקולאַרע סיסטעם, אַרייַנגערעכנט פֿאַרבעסערן בלוט-געבראַכטע באַריערע דורכדרינגלעכקייט, פּראָמאָטירן אַנדזשיאָגענעסיס, און רעדוצירן עדעמאַ. אין דערצו צו צושטעלן געוואקסענע זויערשטאָף צושטעל צו געוועבן, HBOTפֿאַרשטאַרקט וואַסקולאַרע פאָרמאַציעדורך אַקטיווירן טראַנסקריפּציע פאַקטאָרן ווי וואַסקולאַר ענדאָטעליאַל גראָוט פאַקטאָר און דורך סטימולירן די פּראָליפעריישאַן פון נעוראַל סטעם סעלז.
4. עפּיגענעטישע עפֿעקטן פֿון HBOT
שטודיעס האבן אַנטפּלעקט אַז אויסשטעל פון מענטשלעכע מיקראָוואַסקולאַר ענדאָטעליאַל צעלן (HMEC-1) צו היפּערבאַריש זויערשטאָף רעגולירט באַדייטנד 8,101 גענען, אַרייַנגערעכנט ביידע אַפּראָוטשט און דאַונרעגולירט אויסדרוקן, וואָס הויכפּונקט אַ פאַרגרעסערונג אין גען אויסדרוק פֿאַרבונדן מיט אַנטיאַקסאַדאַנט ענטפער פּאַטווייז.
מסקנא
די נוצֿונג פֿון HBOT האָט געמאַכט באַדײַטנדיקע פֿאָרשריט מיט דער צײַט, באַווײַזנדיק זײַן פֿאַרפֿיגבאַרקייט, פֿאַרלעסלעכקייט און זיכערקייט אין קלינישער פּראַקטיק. כאָטש HBOT איז געוואָרן אויסגעפֿאָרשט ווי אַן אָפֿ-ליבל באַהאַנדלונג פֿאַר NDDs און עטלעכע פֿאָרשונגען זענען דורכגעפֿירט געוואָרן, בלײַבט פֿאַראַן אַ דרינגענדיקע נויט פֿאַר שטרענגע שטודיעס צו סטאַנדאַרדיזירן HBOT פּראַקטיקעס אין באַהאַנדלען די דאָזיקע צושטאַנדן. ווײַטערדיקע פֿאָרשונג איז וויכטיק צו באַשטימען אָפּטימאַלע באַהאַנדלונג פֿרעקווענצן און אָפּשאַצן די מאָס פֿון נוצבארע עפֿעקטן פֿאַר פּאַציענטן.
אין קורצן, די קנופּ פון היפּערבאַריש זויערשטאָף און נעוראָדעגענעראַטיווע קראַנקייטן דעמאָנסטרירט אַ פּראַמישינג גרענעץ אין טעראַפּעווטישע מעגלעכקייטן, וואָס רעכטפארטיקט ווייטערדיקע אויספאָרשונג און וואַלידאַציע אין קלינישע סעטטינגס.
פּאָסט צייט: 16טן מײַ 2025

